





近日,中国科大苏州高等研究院、生物医学工程学院石发展教授课题组在基于金刚石氮-空位(NV)色心的生物传感方面取得了系列进展,包括与南开大学苏循成教授团队合作首次基于量子弛豫技术实现了单分子水平的生物分子相互作用检测,以及实现了界面上DNA单分子相互作用动力学的可视化实时磁检测。相关研究成果分别以“Quantum relaxometry for detecting biomolecular interactions with single NV centers”为题发表于《美国国家科学院院刊》(Proc Natl Acad Sci USA)和以“Magnetic monitoring of single-DNA interaction dynamics at interfaces using diamond quantum sensors”为题发表于《纳米快报》(Nano Letters)。
生物分子之间的相互作用是生命活动的基础。在单分子水平研究这些相互作用,可以揭示系综水平检测所无法捕捉的分子个性化特征,对于生命科学具有重要意义。目前常用的单分子荧光技术易受光漂白和背景荧光干扰,而纳米孔技术则容易受到溶液中其他分子或离子的影响。相比之下,自旋信号和磁信号具有稳定性高、生物背景干扰低等显著优势,为单分子检测提供了新路径。
自旋信号检测通常采用磁共振技术,然而传统磁共振依赖感应线圈作为传感器,无法实现单分子灵敏度。近年来金刚石NV色心成为新兴的量子传感器,具有优异的自旋检测灵敏度和生物相容性,已在单个蛋白质分子和核酸分子等检测方面取得突破并展现出潜力[Rev. Mod. Phys. 96, 025001 (2024)]。但进一步解析生物分子间的相互作用仍面临重大挑战,其中关键问题是如何在实现金刚石量子传感器表面高效率分子修饰的同时保持生物分子的活性,这一挑战源于金刚石惰性表面和空间位阻干扰。
针对该问题,在第一项研究中,研究团队设计构建了聚乙烯亚胺纳米凝胶界面,成功在金刚石表面实现了高密度(平均蛋白间距~10纳米)且低空间位阻的生物分子修饰。同时还提出一种“加权弛豫速率”分析方案,充分挖掘了以往被忽视的、对表面分子自旋信号更敏感的快速弛豫分量,检测灵敏度相较传统分析方式提升约4倍,为微弱生物分子相互作用检测提供了一种普适的分析工具。结合金属自旋标记方法(如Gd³⁺, Mn²⁺标记),团队以链霉亲和素和Mn2+标记的生物素-泛素蛋白复合物为例,实现了从微米到纳米尺度的生物分子相互作用高灵敏量子弛豫检测技术(图1)。该技术具有两方面的显著特点:单NV色心可实现优于10纳米的空间分辨率,具备单分子检测能力;金属自旋标记的光稳定性高(可连续观测15小时无明显衰减),远超荧光标记,支持长时间动态监测。未来,该技术可与纳米柱阵列、微流控等系统结合,发展成高通量、低样品消耗的分析平台,为疾病标志物超灵敏检测及药物筛选等提供新方式,推动量子生物传感技术迈向实际应用。
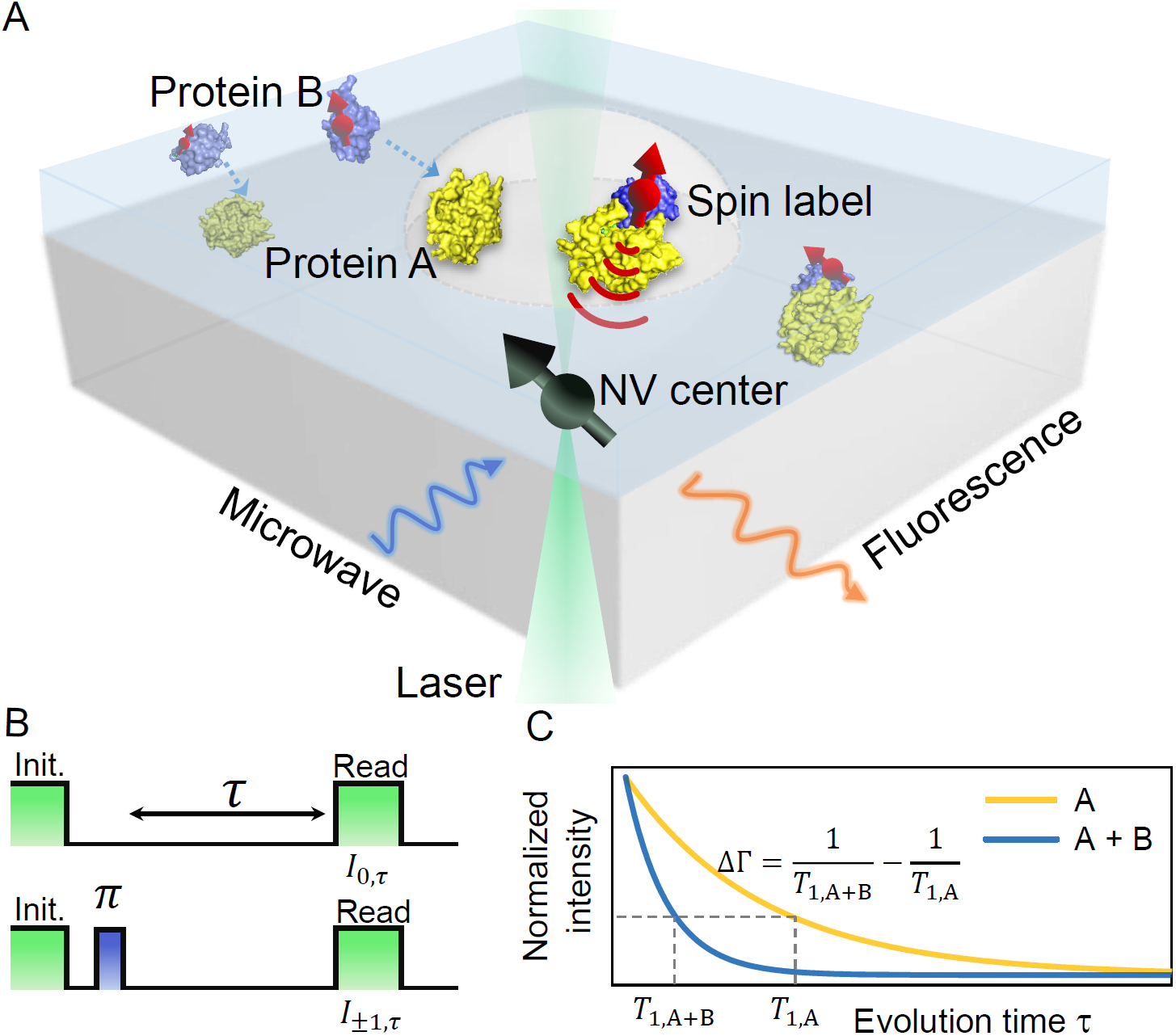
图1. 基于量子弛豫技术的分子相互作用检测。
在第二项研究中,研究团队利用磁纳米颗粒,在前期建立的基于金刚石NV色心的单颗粒磁成像技术(SiPMI)[Nano Letters 23(7), 2636-2643 (2023)]的基础上,从静态推进到动态,首次实现了动态单颗粒磁成像技术(dSiPMI)。在生理溶液中,团队利用该技术成功对磁纳米颗粒与金刚石的功能化表面间的DNA杂交动力学实现了可视化实时检测(图2),并提取出DNA相互作用的特征动力学参数,尤其是单分子相互作用过程。在此基础上,团队对不同Na+浓度条件下的单分子水平DNA杂交过程开展了长达1小时的连续监测,展现了新方法的鲁棒性和实际应用价值。该研究确立了一种可靠的单分子磁学新方法,可以用于不同生理环境下单分子相互作用的实时、长时程和高稳定观测,在细胞生理过程和生物医学高灵敏检测中的分子动力学研究方面具有重要应用价值,尤其适用于界面上的生物分子相互作用分析。
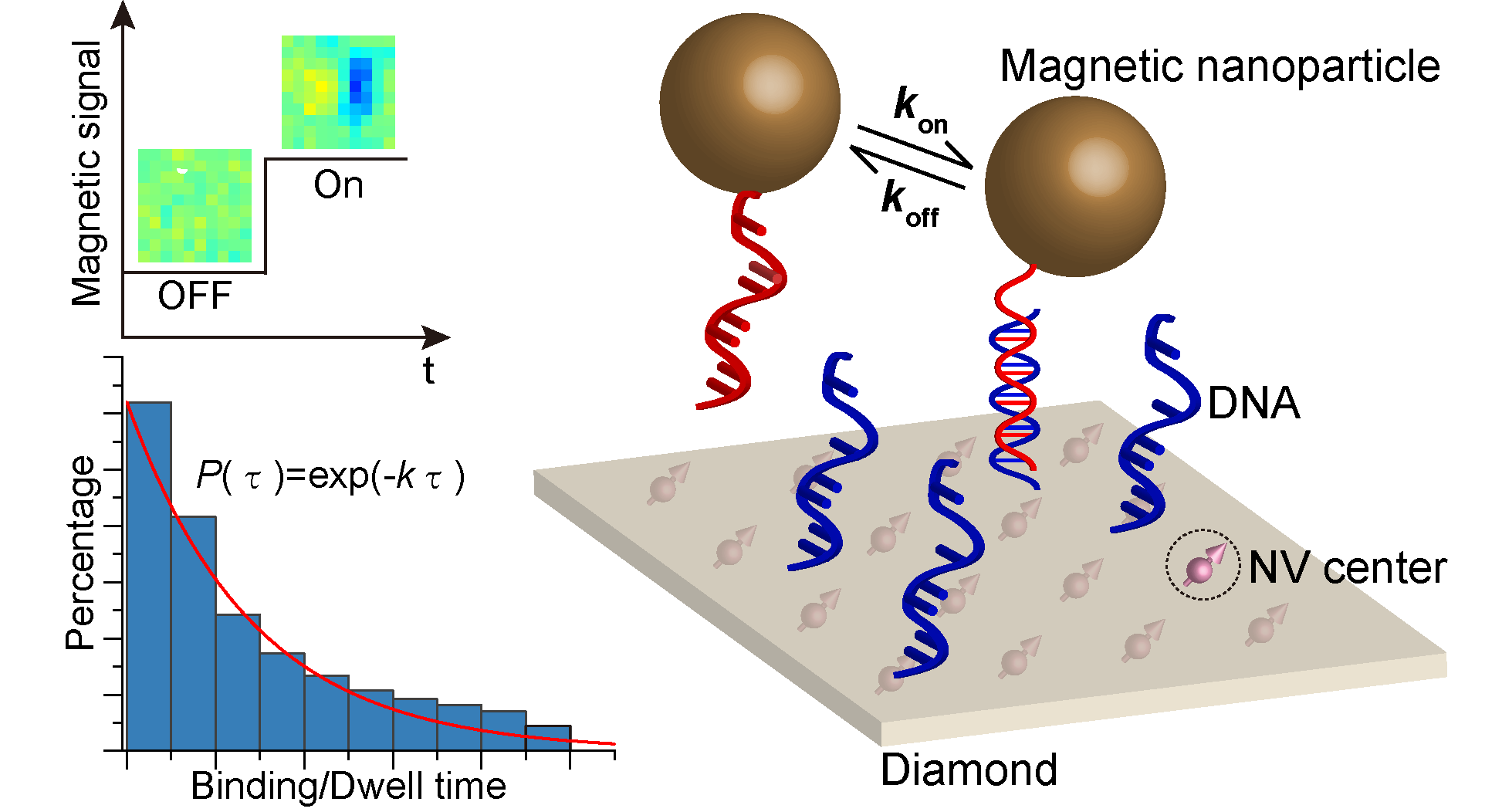
图2. 基于动态单颗粒磁成像的界面单分子相互作用检测。
第一项研究的第一作者为博士后李敏,通讯作者为张琪研究员、苏循成教授和石发展教授;第二项研究的第一作者为博士后孙梓庭,通讯作者为陈三友特任研究员和石发展教授,博士后李万和参与了该研究。上述研究得到了科技部、国家自然科学基金委、中国科学院、安徽省、江苏省和苏州市等单位的支持。
论文链接:
https://www.pnas.org/doi/10.1073/pnas.2509102122
https://pubs.acs.org/doi/10.1021/acs.nanolett.5c03522